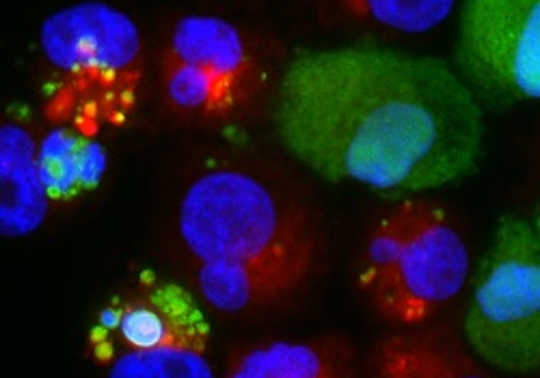
स्तन कैंसर की मौत की दर समग्र रूप से 1989 के बाद से लगातार गिरावट आई है, जो एक से आगे बढ़ रही है बचे लोगों की बढ़ती संख्या। लेकिन जब स्तन कैंसर के बचे लोग आभारी होते हैं तो उनके शरीर रोग का कोई निशान नहीं दिखाते हैं, फिर भी वे चिंता का सामना करते हैं। स्तन कैंसर कर सकते हैं और वापसी करता है, कभी-कभी प्रतिशोध के साथ, यहां तक कि कई वर्षों से छूट के बाद भी। ![]()
कैंसर कोशिकाओं की "कैनाबिलिस्टिक" प्रवृत्ति का अध्ययन करके, मेरी शोध टीम ने यह जानने में कुछ प्रगति की है कि क्यों
पुनरावृत्ति और रोग के परिणामों की संभावना कैंसर के हिसाब से भिन्न है उप-प्रकार। लगभग एक तिहाई रोगियों का निदान तीन नकारात्मक स्तन कैंसर, सबसे आक्रामक उपप्रकार, शरीर के दूसरे भाग में पुनरावृत्ति का अनुभव कर सकता है। इसे दूर पुनरावृत्ति कहा जाता है
यह असंभव नहीं है, यह भविष्यवाणी करने के लिए मुश्किल हो गया है कि अगर वही कैंसर फिर से होगा और इसे रोकना होगा। आवर्ती रोग सिर्फ एक कैंसर सेल से पैदा हो सकता है जो प्रारंभिक उपचार से बच गया और निष्क्रिय हो गया। निष्क्रियता ने शरीर में कहीं छिपाने की अनुमति दी, न कि बढ़ते समय या किसी अप्रत्याशित मात्रा में नुकसान के कारण।
इन निष्क्रिय कोशिकाओं को "नींद" करने के लिए क्या निर्धारित करता है और क्या उन्हें "जाग" करने के लिए उत्तेजित करता है और अनियंत्रित तरीके से गुणा करने से शुरु होता है, जिससे नैदानिक माध्यमिक कैंसर निदान को रोकने के लिए महत्वपूर्ण नए उपचार हो सकते हैं।
हाल ही में, मेरी शोध टीम और मैं पर्दाफाश कई सुराग यह समझा सकता है कि इन स्तन कैंसर कोशिकाओं को निष्क्रिय होने के बाद क्या हो सकता है और फिर "भरोसा"। हमने दिखाया कि कोशिका नरभक्षण को निष्क्रियता से जोड़ा गया है
हड्डी स्टेम कोशिका स्तन कैंसर को कैसे प्रभावित करती है?
स्तन कैंसर स्तन या अन्य अंगों, जैसे कि फेफड़े और हड्डी में पुनरावृत्ति कर सकते हैं। जहां स्तन कैंसर बढ़ने का फैसला किया जाता है, यह बड़े पैमाने पर माइक्रोएन्नेरमेंट पर निर्भर करता है। यह उन कोशिकाओं को संदर्भित करता है, जिनमें प्रतिरक्षा कोशिकाओं, रक्त वाहिकाओं, फाइब्रोब्लास्ट्स और अन्य कारकों के बीच चयन प्रोटीन शामिल कोशिकाओं शामिल हैं।
एक सदी पहले, स्टीफन पैगेट नामक एक सर्जन मशहूर तुलना में बीज और मिट्टी के लिए कैंसर मेटास्टेसिस का अंग विशिष्ट प्रसार चूंकि स्तन कैंसर अक्सर हड्डियों में पुनरुत्थान करता है, इस रूपक में, जो अभी आज भी धारण करता है, अस्थि मज्जा सुदृढ़ स्तन कैंसर कोशिकाओं ("बीज") के लिए एक सुक्ष्म microenvironment ("मिट्टी") प्रदान करता है जो कि कामयाब होता है।
इस प्रकार, का एक महत्वपूर्ण राशि हाल ही में किया गया कार्य एक विशेष प्रकार के सेल के कैंसर की निष्क्रियता में भूमिका निर्धारित करने की कोशिश कर रही है, जिसे मेसेनचिमल स्टेम सेल (एमएससी) कहा जाता है। ये अस्थि मज्जा में पाए जाते हैं
अस्थि मज्जा में एमएससी अत्यधिक बहुमुखी हैं वे हड्डियों, उपास्थि और रेशेदार ऊतकों को बनाने में सक्षम हैं, साथ ही साथ कोशिकाओं जो प्रतिरक्षा प्रणाली का समर्थन करते हैं और रक्त का गठन करते हैं। वे भी यात्रा करने के लिए जाना जाता है ऊतक की चोट और सूजन की साइटों, जहां वे उपचार में सहायता करते हैं।
स्तन कैंसर कोशिकाओं आसानी से बातचीत करें एमएससी के साथ यदि वे अस्थि मज्जा में मिलते हैं अगर स्तन कैंसर की कोशिकाओं ने उन्हें प्राथमिक ट्यूमर के स्थान पर भर्ती किया है तो वे आसानी से बातचीत करते हैं
मेरी शोध टीम और मैंने हाल ही में इन सेलुलर इंटरैक्शन के संभावित परिणामों पर ध्यान केंद्रित किया। हमें एक अजीब चीज मिलती है, जिससे ये पता चलता है कि ये स्तन कैंसर की कोशिकाएं कितनी देर तक छिप रही हैं।
प्रयोगशाला की सेटिंग में, हमने स्तन ट्यूमर मॉडल का उत्पादन किया जिसमें एमएससी शामिल था। हमने शत्रुतापूर्ण स्थितियों को फिर से बनाया है जो स्वाभाविक रूप से मरीजों में ट्यूमर को विकसित करने के लिए चुनौती देते हैं, जैसे कि कैंसर कोशिकाओं के तेजी से विकास और भीड़ से बढ़ने के कारण स्थानीयकृत पोषक तत्व घाटे।
हमने खोजा कि इस दबाव के तहत कैंसर की कोशिकाओं खाने के बाद निष्क्रिय हो, या "cannibalizing," स्टेम कोशिकाओं।
हमारा विश्लेषण प्रदान किया गया सम्मोहक डेटा दिखा रहा है कि कैनिबैलिस्टिक स्तन कैंसर की कोशिकाओं के रूप में ट्यूमर के रूप में तेजी से अन्य कैंसर कोशिकाओं के रूप में नहीं, और कभी कभी बिल्कुल नहीं था उसी समय, वे बन गए अत्यधिक प्रतिरोधी पोषक तत्वों के अभाव द्वारा लगाए गए केमोथेरेपी और तनाव के लिए
निष्क्रिय कोशिकाओं को पुनरावृत्ति से व्यापक रूप से जोड़ा जाता है। हम इस परिकल्पना करते हैं कि नरभक्षण इस प्रकार पुनरावृत्ति से जुड़ा हुआ है।
सेलुलर नरभक्षण क्या है, और यह कैंसर में क्यों महत्वपूर्ण है?
सेलुलर नेनिबिलिज़्म, सामान्य रूप में, एक अलग घटना का वर्णन करता है जिसमें एक कोशिका पड़ोसी, अक्षत कोशिकाओं को खत्म करती है और समाप्त करती है।
कैंसर कोशिकाओं का प्रतिशत जो cannibalistic गतिविधि दिखाता है अपेक्षाकृत कम है, लेकिन यह बढ़ने लगता है अधिक आक्रामक ट्यूमर में
कई कारण हैं कि स्तन कैंसर कोशिकाएं अन्य कोशिकाओं को खाने के लिए चाहती हैं, जिनमें अन्य कैंसर कोशिकाओं भी शामिल हैं। यह उन्हें पोषक तत्वों की कम आपूर्ति के दौरान खिलाने का एक तरीका प्रदान करता है। यह उन्हें एक तरीका भी प्रदान करता है बहुत प्रतिरक्षा कोशिकाओं को खत्म कि प्राकृतिक रूप से कैंसर के विकास को रोकना सेल नरभक्षण भी कैंसर कोशिकाओं को नई अनुवांशिक जानकारी प्राप्त करने की अनुमति दे सकता है और इसलिए, नए और लाभप्रद लक्षण।
विशेष रूप से, में हमारे अध्ययन, नशे की लत स्तन कैंसर की कोशिकाओं जो स्टेम सेल खाती हैं और निद्रा में प्रवेश किया विशिष्ट प्रोटीन की एक सरणी का उत्पादन करना शुरू कर दिया इनमें से कई प्रोटीनों को सामान्य कोशिकाओं द्वारा भी स्रावित किया जाता है जो कि स्थायी रूप से विभाजित करना बंद कर देते हैं, या सीनेस्केंट कोशिकाएं, और सामूहिक रूप से करार दिया la सिनेंसेन से जुड़ी सिक्योरिटी फेनोटाइप (या एसएपी) हालांकि सेलुलर senescence उम्र बढ़ने का एक हिस्सा है, हम अब महसूस कर रहे हैं कि यह भी विभिन्न शारीरिक प्रक्रियाओं, भ्रूण और वयस्कों में चोट की मरम्मत के विकास के लिए भी महत्वपूर्ण है।
इससे पता चलता है कि हालांकि निष्क्रिय कैंसर कोशिकाओं को तेजी से गुणा नहीं पड़ता है या पता लगाने योग्य ट्यूमर बना सकता है, लेकिन ये जरूरी नहीं कि सो रहे हैं। इसके बजाय, कई बार वे सक्रिय रूप से एक-दूसरे के साथ संवाद कर सकते हैं और उनके प्रोटीन के निर्माण के माध्यम से उनके माइक्रोएनेवाइनमेंट का निर्माण कर सकते हैं।
कुल मिलाकर, यह निष्क्रिय कैंसर कोशिकाओं के लिए "रडार के नीचे उड़ान भरने" के लिए एक चतुर तरीका हो सकता है, और साथ ही, अपने माइक्रोएनेरमेंचर को संशोधित कर सकता है, जिससे भविष्य में उन्हें बढ़ने के लिए इसे और अधिक उपयुक्त बनाया जा सकता है।
निदान और उपचार के लिए सेल नरभक्षण का फायदा उठाया जा सकता है?
यद्यपि हमारे परिणाम आशाजनक हैं, सावधान रहना महत्वपूर्ण है। जबकि सेल नरभक्षण और निद्रा के बीच एक मजबूत संबंध प्रतीत होता है, अब हम नहीं जानते कि क्या यह सीधे रोगियों में कैंसर पुनरावृत्ति से जुड़ा हुआ है। हालांकि, हमारे निष्कर्षों की पुष्टि करने के लिए अध्ययन चल रहे हैं
फिर भी, तथ्य यह है कि स्तन कैंसर की कोशिकाओं एमएससी की cannibalize दिलचस्प है। यह नए नैदानिक उपकरण और चिकित्सा विकसित करने के लिए एक महत्वपूर्ण आधार प्रदान करता है। दरअसल, हमारे वर्तमान में हमारे हालिया खोजों को लागू करने के कई तरीके हैं
एक रोमांचक विचार कैंसर की कोशिकाओं की कैनीबैलिस्टिक गतिविधि का फायदा उठाने के लिए उन्हें आत्मघाती जीन या अन्य जहरीले एजेंटों को खिलाने के लिए है, एमएससी को डिलीवरी वाहन के रूप में, ट्यूमर की तलाश करने वाली मिसाइल की तरह।
महत्वपूर्ण बात, एमएससी को आसानी से शरीर से प्राप्त किया जा सकता है, प्रयोगशाला में बड़ी संख्या में विस्तार किया जा सकता है, और रोगी को वापस कर सकता है। वास्तव में, वे पहले से ही सुरक्षित रूप से उपयोग किए जा चुके हैं क्लिनिकल परीक्षण ऊतक की मरम्मत और पुनर्जन्म में सहायता करने की उनकी क्षमता के कारण विभिन्न बीमारियों का इलाज करना
नशीली दवाओं के विकास के लिए एक अलग एवेन्यू में निष्क्रिय कोशिकाओं को एक हानिरहित और नाबालिग राज्य में कायम रखना शामिल होगा। कैंसर की कोशिकाओं को पहली जगह में स्टेम सेल खाने से रोकना संभव हो सकता है
हमारे अध्ययन में, हम कैंसर कोशिकाओं के अंदर एक विशेष प्रोटीन को लक्षित करने वाली एक दवा का उपयोग करके सेल नरभक्षी को रोकने में सक्षम थे। इस उपचार के दृष्टिकोण के साथ, कैंसर मूल रूप से मौत के शिकार हो सकता है या परंपरागत चिकित्सा द्वारा आसानी से मारे जा सकता है।
के बारे में लेखक
थॉमस बार्टोश, सहायक प्रोफेसर, कॉलेज ऑफ मेडिसिन, टेक्सास ए एंड एम विश्वविद्यालय
यह आलेख मूलतः पर प्रकाशित हुआ था वार्तालाप। को पढ़िए मूल लेख.
संबंधित पुस्तकें
at इनरसेल्फ मार्केट और अमेज़न

























