20th सदी की शुरुआत में, Alois अल्जाइमर पहले एक 50-वर्षीय महिला में प्रगतिशील स्मृति हानि और भ्रम की स्थिति का वर्णन किया। उसके मरने के बाद, उसने उसके मस्तिष्क की जांच की और देखा कि यह असामान्य प्रोटीन के थक्कों से भरा था, जिसे सजीले टुकड़े के रूप में जाना जाता है। एक सदी बाद, हम जानते हैं कि ये सजीले टुकड़े बीटा-एमाइलॉइड नामक एक प्रोटीन से भरे हुए हैं और इस बीमारी की एक बानगी है जो अल्जाइमर का नाम है। जबकि अल्जाइमर रोग की अन्य विशेषताओं का पता चला है, सिद्धांत है कि बीटा-अमाइलॉइड इस लाइलाज बीमारी का मुख्य कारण है।
"बीटा-एमाइलॉयड परिकल्पना" के कई सूक्ष्म रूपांतर हैं, लेकिन आम तौर पर यह सिद्धांत जाता है कि बीटा-एमिलॉइड मस्तिष्क में जमा होता है, फिर एक साथ चिपक जाता है। इस प्रक्रिया में कहीं-कहीं मस्तिष्क की तंत्रिका कोशिकाएँ क्षतिग्रस्त हो जाती हैं, जिससे स्मृति हानि और अल्जाइमर रोग के अन्य लक्षण उत्पन्न हो जाते हैं। इसलिए इसका इलाज करने का तरीका सीधा होना चाहिए: अकड़ना बंद करें और आप इस बीमारी को रोक देंगे।
दुर्भाग्य से, दशकों के अनुसंधान, कई मिलियन डॉलर के निवेश और कई असफल नैदानिक परीक्षण बाद में, ऐसा प्रतीत होता है कि यह दृष्टिकोण काम नहीं कर रहा है। निराशाजनक परिणाम उत्पन्न करने के लिए सबसे हालिया पट्टिका-विक्षोभ उपचार aducanumab रहा है - एक एंटीबॉडी-आधारित थेरेपी जिसे बीटा-एमिलॉइड से चिपके और नष्ट करने के लिए डिज़ाइन किया गया है।
प्रारंभिक आंकड़ों ने सुझाव दिया कि उपचार ने वास्तव में, मस्तिष्क से बीटा-एमिलॉइड को स्पष्ट किया। लेकिन इस सप्ताह, एडोजेनमबब के पीछे दवा कंपनियों बायोजेन और ईसाई, क्लिनिकल परीक्षण समाप्त हजारों रोगियों को जल्दी शामिल करना, बताते हुए कि "परीक्षण पूरा होने पर अपने प्राथमिक समापन बिंदु को पूरा करने की संभावना नहीं थी"।
इसने कई लोगों से पूछा है कि क्या अल्जाइमर रोग के अमाइलॉइड परिकल्पना को छोड़ दिया जाना चाहिए। वास्तव में, कुछ न्यूरोसाइंटिस्ट अभी भी इस दृष्टिकोण की सदस्यता लेते हैं कि यह बीटा-एमाइलॉयड प्लेक है जो अल्जाइमर रोग के लक्षणों का कारण बनता है।
मानव अल्जाइमर रोग की नकल करने वाले चूहों के साथ अध्ययन से पता चला है कि मस्तिष्क में सजीले टुकड़े बनने से पहले स्मृति हानि होती है। अन्य अध्ययनों ने सुझाव दिया है कि यह बीटा-एमिलॉइड के छोटे टुकड़े ("ओलिगोमर्स") है जो वास्तव में तंत्रिका कोशिकाओं के लिए विषाक्त हैं। और यह भी सुझाव दिया गया है कि सजीले टुकड़े का निर्माण मस्तिष्क के लिए सुरक्षा के लिए इन सभी खतरनाक ओलिगोमर्स को एक स्थान पर गोल-अप करने का एक तरीका है।
यह बहुत कठिन है कि एडुकानुमाब परीक्षण से पूरी जानकारी के बिना बताएं, लेकिन शायद उपचार के प्रभावी होने के लिए प्रतिभागियों में यह बीमारी बहुत आगे बढ़ गई थी। शायद छोटे बीटा-एमिलॉइड ओलिगोमर्स ने पहले ही अपना नुकसान कर लिया था, प्रतिभागियों को परीक्षण के लिए भर्ती करने से पहले इस बीमारी को गति में स्थापित किया।
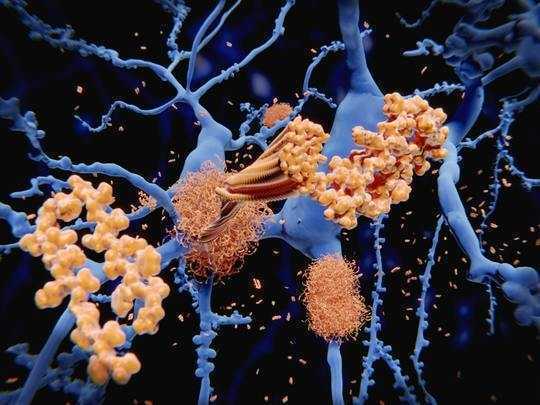 मस्तिष्क कोशिकाओं (नीला) के चारों ओर अमाइलॉइड-बीटा प्लेक (पीला) क्लंपिंग। जुआन गर्टनर / शुटरस्टॉक
मस्तिष्क कोशिकाओं (नीला) के चारों ओर अमाइलॉइड-बीटा प्लेक (पीला) क्लंपिंग। जुआन गर्टनर / शुटरस्टॉक
अल्जाइमर रोग अल्जाइमर डिमेंशिया
हाल ही में अल्जाइमर रिसर्च यूके कॉन्फ्रेंस में, सार्वभौमिक समझौते के पास था कि अल्जाइमर रोग की अवधारणा को मनोभ्रंश से अलग करने का समय आ गया है।
अल्जाइमर रोग को बीटा-एमिलॉइड सजीले टुकड़े के निर्माण और दूसरे प्रोटीन के ताऊ के रूप में परिभाषित किया गया है, ताऊ, जो कुछ हल्के स्मृति परिवर्तनों के साथ संयुक्त है। डिमेंशिया इस बीमारी का एक लक्षण है। मस्तिष्क इमेजिंग में अग्रिम का मतलब है कि डॉक्टर अब अल्जाइमर रोग के इन संकेतकों को बहुत पहले (25 साल पहले मनोभ्रंश के लक्षणों में सेट होने तक) देख सकते हैं। आश्चर्यजनक रूप से अंडर-रिपोर्ट तथ्य यह है कि मनोभ्रंश को प्रगति एक दिया नहीं है। सभी लोग जो अल्जाइमर रोग के इन नैदानिक संकेतों को नहीं दिखाते हैं, उनके जीवन काल में मनोभ्रंश की प्रगति होगी।
हम केवल उन कारणों का अध्ययन करने लगे हैं जो अल्जाइमर रोग वाले कुछ लोग अल्जाइमर डिमेंशिया से बचते हैं। इस प्रगति के लिए आयु सबसे बड़ा जोखिम कारक है; जब आप बीटा-अमाइलॉइड को मस्तिष्क में बनाना शुरू करते हैं, तो आप डिमेंशिया से पीड़ित होने की अधिक संभावना रखते हैं। आहार, शिक्षा और सिर की चोटें भी इस प्रक्रिया में एक भूमिका निभा सकती हैं, लेकिन हम किस हद तक नहीं जानते हैं।
एक अन्य प्रमुख कारक जिसे हम केवल समझने की शुरुआत कर रहे हैं वह है आनुवंशिकी। हमारे जीन में छोटे बदलाव न केवल प्रभावित करने के लिए प्रतीत होते हैं कि क्या हम मस्तिष्क में बीटा-एमिलॉइड का निर्माण करेंगे, लेकिन क्या उस संचय से मनोभ्रंश लक्षण होते हैं।
हालांकि, इन तथाकथित "जोखिम जीन" को खोजने की प्रक्रिया धीमी है। प्रगति ज्यादातर "बड़े डेटा" अध्ययनों से आई है जो मानव जीनोम के दो अरब विषम डीएनए ठिकानों में हजारों लोगों के बीच छोटे बदलावों को ट्रैक करते हैं और अल्जाइमर के इन परिवर्तनों और दरों के बीच पैटर्न खोजने की कोशिश करते हैं।
मानव जीनोम के लगभग 30 क्षेत्र हैं जिन्हें अल्जाइमर डिमेंशिया के विकास के जोखिम से जोड़ा गया है, हालांकि निश्चित रूप से और अधिक खोज की जानी है।
Aducanumab: सही इलाज, गलत समय?
जैसे कि कई अन्य मानव रोगों के लिए उपचार के साथ, यह हो सकता है कि एडुकानुमाब जैसे उपचार केवल तभी प्रभावी हो सकते हैं जब उन्हें पर्याप्त रूप से दिया जाए, इससे पहले कि बीमारी अपरिवर्तनीय परिवर्तन हो। अल्जाइमर रोग के पीछे पर्यावरण और आनुवांशिक कारकों की बेहतर समझ, कभी अधिक संवेदनशील मस्तिष्क इमेजिंग तकनीकों के साथ संयुक्त रूप से डॉक्टरों को चेतावनी के संकेतों की पहचान करने में मदद करेगी, इससे पहले कि मामूली स्मृति हानि भी हो।
लोगों की जांच और निदान करते समय - इससे पहले कि लक्षणों में - एक अभी तक लाइलाज बीमारी के लिए निर्धारित किया गया है, कई नैतिक दुविधाओं को उठाता है, यह बीटा-एमिलॉइड दवाओं को पुन: उपयोग करने के लिए अवसर की एक नई खिड़की पेश कर सकता है, जैसे कि एडुकेमबब। अंतत: हमें बीमारी के शुरुआती चरणों को समझने के लिए अपने शोध पर ध्यान केंद्रित करने की आवश्यकता है ताकि हम अल्जाइमर रोग को रोक सकें, इससे पहले कि डिमेंशन न हो।![]()
के बारे में लेखक
विक्की जोन्स, सेल बायोलॉजी में वरिष्ठ व्याख्याता, सेंट्रल लंकाशायर विश्वविद्यालय
इस लेख से पुन: प्रकाशित किया गया है वार्तालाप क्रिएटिव कॉमन्स लाइसेंस के तहत। को पढ़िए मूल लेख.
संबंधित पुस्तकें:
at इनरसेल्फ मार्केट और अमेज़न